Aus dem Venenzentrum Frankfurt am Main
(Prof. Dr. V. Hach-Wunderle, Prof. Dr. W. Hach)
Ist die Venenkrosse nicht mehr wichtig?
Die Bedeutung der Krossektomie für die konventionelle und endovasale Chirurgie der Stammvarikose
Die Geschichte der Chirurgie hat uns gelehrt, dass die Trendelenburg´sche Konzeption der solitären Saphena-Ligatur beim Privatkreislauf der Stammvarikose aus prinzipiellen Gründen nicht erfolgreich sein kann, weil es sich beim Venensystem im Gegensatz zu den Arterien um ein Netzwerk handelt. Aus dieser Erkenntnis hat sich schließlich die operative Behandlung der schweren Krampfaderkrankheit durch Krossektomie und Stripping weltweit durchgesetzt. Die endovasalen Operationsmethoden der Radiowellen-Ablation und der Laser-Koagulation stellen heute die Krossektomie prinzipiell in Frage. Prospektive Studien zu diesem Thema liegen nicht vor. Deshalb wird versucht, aus den vergleichenden Daten der Literatur eine Bewertung herbeizuführen.
Untersuchungen und Ergebnisse. Im Mittelpunkt stehen die klassischen Follow-up-Studien von Hach (1981) sowie von Stranzenbach und Hach (1991), nach denen auf Grund phlebographischer Kriterien und von Ergebnissen der peripheren Phlebodynamometrie das Phänomen der sekundären Leitveneninsuffizienz ganz in den Vordergrund tritt. In den Stadien I und II einer Stammvarikose der V. saphena magna sind keine morphologischen und pathophysiologischen Veränderungen im tiefen Venensystem zu erwarten. In den Stadien III und IV muss dagegen mit der Entwicklung der sekundären Leitveneninsuffizienz gerechnet werden, die den Patienten in die chronische venöse Insuffizienz führt.
Schlußfolgerung. In der Therapie der Stadien I und II einer Stammvarikose der V. saphena magna kommt es auf die Beseitigung der Varikose an, ganz gleich auf welche Weise. In den Stadien III und IV lässt sich die Gefahr der sekundären Leitveneninsuffizienz nach den bisherigen Kenntnissen nur durch die komplette Ausschaltung des Rezirkulationskreises verhindern, und die Krossektomie gehört unabdingbar dazu. Dem Argument der Neovaskularisation wird nur eine geringe klinische Relevanz zuerkannt. Wichtig erscheint dagegen die schon präoperativ nachweisbare Existenz eines inguinalen Varizenbeets, das bei unvollständiger Krossektomie und bei der Möglichkeit des Anschlusses an einen gedoppelten peripheren Stamm der V. saphena magna eine komplikationsträchtige Rezidivvarikose nach sich ziehen kann.
Venenstamm-ausschaltende Maßnahmen
Laser-Obliteration
Schaumsklerosierung
Venenstamm-erhaltende Operationen
CHIVA
Den Zündstoff dafür lieferten die Forderungen nach Minimalisierung des Eingriffs und die hohen Ansprüche in ästhetischer Hinsicht. Eine chirurgische Ausbildung des behandelnden Arztes ist nicht mehr unbedingt erforderlich. Der Patient kann in der Regel auf die Unterbrechung der Arbeit und auf einen Klinikaufenthalt verzichten. Es ist auch in Betracht zu ziehen, dass zur objektiven Untersuchung der morphologischen und der hämodynamischen Situation früher invasive Verfahren wie die Phlebographie und die periphere Phlebodynamometrie zur Anwendung gelangten, während heute die Diagnostik meistens auf der Sonographie und allenfalls noch zusätzlich auf der Plethysmographie beruht (15). Nicht zuletzt wird im Sinne der neuen Operationsverfahren ohne Krossektomie argumentiert, dass durch die hohe Quote von Krosse-Rezidiven bis zu 60% (3, 4) „das Dogma der chirurgischen Behandlung von Krampfadern erstmals ins Wanken“ geriet (S. Guggenbichler und FX. Breu auf dem Sklerotherapie-Symposium am 4.-6- April 2003 am Tegernsee).
Wie aber steht es um die wissenschaftlichen Begründungen der Krossektomie? In der vorliegenden Arbeit sollen wichtige Erkenntnisse der konventionellen Operationstechnik ins Gedächnis gerufen und dann am Beispiel der Radiofrequenz-Ablation sowie der endovasalen Laser-Koagulation jeweils ohne Krossektomie erörtert werden.
Historische Einführung
Die ersten wissenschaftlichen Betrachtungen zum Krankheitsbild der Stammvarikose gehen auf Fritz Trendelenburg (1844-1924), Ordinarius für Chirurgie in Berlin, Bonn und Leipzig zurück (32). Er beschrieb im Jahre 1891 seinen „Privatkreislauf“, und die logische Konsequenz dieser Theorie führte zur Operationsmethode der Saphena-Ligatur am Oberschenkel. Heute wissen wir, dass der entscheidende Denkfehler von Trendelenburg darin bestand, das Venensystem nicht wie ein Netzwerk, sondern wie einen Gefäßbaum entsprechend dem arteriellen System zu verstehen. Typisch für den netzartigen Aufbau von vaskulären Strukturen ist die unendlich große Möglichkeit der Kompensation eines Gefäßverschlusses durch anatomisch präformierte Kollateralen.
Schon Georg Perthes (1869-1927), Oberarzt bei Trendelenburg und später Ordinarius für Chirurgie in Leipzig und Tübingen, musste bei Kontrolluntersuchungen nach durchschnittlich 4 Jahren (5 Monate bis 9 Jahre) feststellen, dass bei 9 von 41 Patienten schwere Rezidive aufgetreten waren. Er forderte deshalb, „dass ein Stück der Saphena reseciert werde und das Operationsfeld möglichst hoch hinauf zu legen“ ist (27).
Nach meinen Recherchen wurde die Krossektomie im heutigen Sinne an der Chirurgischen Klinik zu Genua um die Jahrhundertwende eingeführt. Der Assistenzarzt Prof. Dr. G. Moro beschrieb 1910 das operative Verfahren seines Chefs Senator Prof. Dr. G. F. Novaro auf der Grundlage der Trendelenburg´schen These und bemerkenswerter eigener pathophysiologischer Betrachtungen (23). „Die Vena saphena magna ist an ihrer Einmündungsstelle zwei Querfinger unterhalb des Poupart´schen Bandes freizulegen, um sie samt ihrer Collateralen gut zu resecieren; auch die Venae pudenda externa, circumflexa ilium superficialis und epigastrica superficialis sind auf eine gewisse Strecke bloßzulegen, um einen eventuell sekundären Blutrückfluß in das System der großen Vena saphena, sowie die Varicenrecidive samt allen Folgen auf diesem Wege hintanzuhalten“.
Rezirkulationskreise und sekundäre Leitveneninsuffizienz
Zum Verständnis der Auswirkungen oder des Verzichts einer Krossektomie auf den Verlauf des Krankheitsbildes der Stammvarikose sind Betrachtungen zur Pathophysiologie unumgänglich. Dazu dienen die Einteilung der Stammvarikose in Stadien sowie die theoretischen Konzepte der Rezirkulationskreise und der sekundären Leitveneninsuffizienz (14, 15).
Einteilung nach Stadien
Die initiale Insuffizienz der Mündungs- und Schleusenklappen der V. saphena magna führt zur varikösen Degeneration des Saphenastamms. In den meisten Fällen betrifft dieser Prozeß aber nicht das ganze Gefäß. Vielmehr endet der insuffiziente Anteil der V. saphena magna fußwärts mit einer kompetenten Venenklappe am distalen Insuffizienzpunkt. Der distale Insuffizienzpunkt I liegt in der Leiste, der Punkt II im Bereich des Oberschenkels, der Punkt III handbreit unterhalb vom Knie und der Punkt IV am Fuß.
Als proximaler Insuffizienzpunkt ist die Stelle der insuffizienten transfaszialen Kommunikation definiert (14). Bei der (kompletten) Stammvarikose der V. saphena magna liegt er in der Leiste. Seine Ausschaltung gilt als zentraler Anspruch der Krossektomie.
Die Stammvarikose ist in einen Rezirkulationskreis eingebunden, der seinen prinzipiellen Aufbau auch nach jahrzehntelangem Krankheitsverlauf nicht verändert. Er kann jedoch dekompensieren und dadurch eine richtungsgebende Verschlimmerung des klinischen Bildes herbeiführen. Deshalb treten die schweren Krankheitssymptome und die Komplikationen erst im späteren Lebensalter des Patienten auf.
Der Rezirkulationskreis einer Stammvarikose der V. saphena magna beginnt mit dem Rückfluss des Blutes in die Stammvene an der Leiste und setzt sich am distalen Insuffizienzpunkt mit dem Übertritt in die konjugierende Seitenastvarikose fort. Über suffiziente Vv. perforantes strömt das Blut dann wieder dem tiefen Venensystem zu. Auf diese Weise sind die Rezirkulationskreise I-IV analog den Stadien der Stammvarikose nachzuvollziehen.
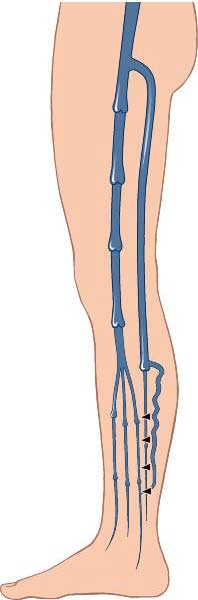
Schematische Darstellung des Rezirkulationskreises III. Erklärung s. Text. (aus Hach et al. VenenChirurgie (15))
Sekundäre Leitveneninsuffizienz
Mit der Zeit werden die tiefen Venen durch das rezirkulierende Blutvolumen überlastet. Sie erweitern sich, bis die Venenklappen nicht mehr schließen, und es entsteht die sekundäre Leitveneninsuffizienz. Der Rezirkulationskreis ist dekompensiert. Das Blut kann durch die Aktivierung der peripheren Venenpumpen nicht mehr schwallartig entleert werden. Der periphere Venendruck fällt bei der Muskelarbeit nicht mehr genügend ab („venöse Hypertonie“), und die venöse Kapazität steigt an. Es gilt der Grundsatz, dass jede Schwellungsneigung der Extremität und die Symptome des chronischen venösen Stauungssyndroms auf die Dekompensation des Rezirkulationskreises hinweisen (15).
 Kinking der V. poplitea rechts infolge sekundärer Leitveneninsuffizienz bei ausgeprägter Stammvarikose der V. saphena magna im Stadium IV. Dauer der Krankheit ca 40 Jahre. Schweres chronisches venöses Stauungssyndrom mit Ulcera cruris.
Kinking der V. poplitea rechts infolge sekundärer Leitveneninsuffizienz bei ausgeprägter Stammvarikose der V. saphena magna im Stadium IV. Dauer der Krankheit ca 40 Jahre. Schweres chronisches venöses Stauungssyndrom mit Ulcera cruris. a. Innenrotation. b seitlich. (aus Hach et al. VenenChirurgie (15))
Zu welchem Zeitpunkt mit der Dekompensation im Einzelfall zu rechnen ist, hängt von verschiedenen Faktoren ab. Eine zentrale Bedeutung kommt der Lokalisation des distalen Insuffizienzpunktes und damit der Länge der konjugierenden Seitenastvarikose zu. Die Strömungsbedingungen verhalten sich in der insuffizienten V. saphena magna grundlegend anders wie in einem Seitenast. Bei der Stammvene handelt es sich um ein geradliniges Gefäß mit einer hohen Transportkapazität. Die Seitenastvarikose zeigt dagegen einen stark geschlängelten Verlauf, der die Flussgeschwindigkeit stark abbremst und die retrograde Blutströmung limitiert. Die lange Seitenastvarikose beim Rezirkulationskreis I verursacht deshalb eine sehr viel geringere hämodynamische Belastung des Beins als die kürzere Ausbildung bei einer Stammvarikose im Stadium III. Das Fehlen der Seitenastvarikose im Rezirkulationskreis IV wirkt sich verheerend aus.
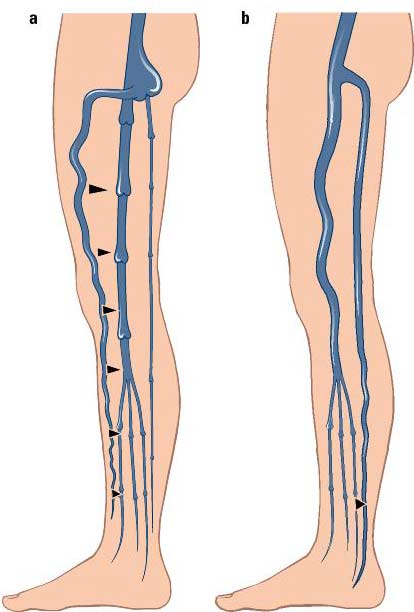 Schematische Darstellung der extremen Rezirkulationskreise.
Schematische Darstellung der extremen Rezirkulationskreise. a. Im Rezirkulationskreis I maximale Ausbildung der Seitenastvarikose und dadurch hämodynamischer Schutz des tiefen Venensystems (aus Hach, VenenChirurgie)
b. Im Rezirkulationskreis IV fehlende konjugierende Seitenastvarikose und deshalb frühzeitige Dekompensation. (aus Hach et al. VenenChirurgie (15))
Die pathologischen Veränderungen in den Leitvenen schreiten fort, so lange der Rezirkulationskreis persistiert. Nach seiner chirurgischen Ausschaltung bilden sie sich weitgehend oder vollständig zurück. Dieser Prozess kann sich über Jahre erstrecken (30, 31).
Die klassischen Follow-up-Studien
Vor Einführung der Sonographie wurden zwei phlebographische Studien vorgelegt, aus denen der Einfluss einer persistierenden sekundären Leitveneninsuffizienz auf den Verlauf der Krampfaderkrankheit abzuleiten ist (14, 31).
Studie. Im Jahre 1981 hat Hach das Verhalten des peripheren dynamischen Venendrucks vor und nach der stadiengerechten Operation einer Stammvarikose der V. saphena magna untersucht. Die Zuordnung der Patienten in Kollektive erfolgte aufgrund der phlebographischen Diagnose. Im Kontrollkollektiv befanden sich 24 venengesunde Probanden. Zum Stadium II gehörten 14, zum Stadium III 15 und zum Stadium IV 29 Patienten. Einer besonderen Gruppe wurden 15 Fälle mit einer Seitenastvarikose der V. saphena accessoria lateralis vom inguinalen supravalvulären Mündungstyp (Stadium I der Stammvarikose) zugeteilt, und ihre Operation bestand in der erweiterten Krossektomie. Der Druckabfall delta-p unterschied sich in den Stadium I und II nicht vom Kontrollkollektiv. In den Stadien III und besonders IV wurden unmittelbar nach der stadiengerechten Operation zwar einer Verbesserung der Druckwerte, aber keine Normalisierung erreicht, denn der dekompensierte Rezirkulationskreis hat ja zunächst noch fortbestanden.
Die Ergebnisse lassen beim heutigen Stand der wissenschaftlichen Kenntnisse folgende Interpretation zu: In den Stadien I (Seitenast-Varikose der V. saphena accessoria lateralis) und II bestanden keine Unterschiede des peripheren dynamischen Venendrucks gegenüber gesunden Probanden. Die Stammvarikose hat zu keinen Veränderungen im Sinne der sekundären Leitveneninsuffizienz geführt. Die Krampfadern spielten in hämodynamischer Hinsicht keine Rolle.
 Verhalten des Druckabfall Dp der peripheren dynamischen Venendruckkurve in einem Kollektiv von venengesunden Probanden und in Patientenkollektiven jeweils vor und nach der Operation einer Stammvarikose der V. saphena magna in den Stadien II, III, und IV. In den schweren Krankheitsstadien kommt es nach der Operation nicht zur Normalisierung der Werte (nach 8).
Verhalten des Druckabfall Dp der peripheren dynamischen Venendruckkurve in einem Kollektiv von venengesunden Probanden und in Patientenkollektiven jeweils vor und nach der Operation einer Stammvarikose der V. saphena magna in den Stadien II, III, und IV. In den schweren Krankheitsstadien kommt es nach der Operation nicht zur Normalisierung der Werte (nach 8).
Studie. Zur Beurteilung des Langzeitverhaltens der sekundären Leitveneninsuffizienz führten Stranzenbach und Hach im Jahre 1991 phlebographische Kontrolluntersuchungen an einem Kollektiv von 14 Patienten mit einer unbehandelten Stammvarikose der V. saphena magna in einer Zeitspanne von durchschnittlich 7,1 Jahren durch. Bei spontanem Krankheitsverlauf nahm der Durchmesser der V. poplitea von 14,6 mm auf 17,6 mm und der V. femoralis superficialis von 14,2 auf 16,4 mm im Durchschnitt zu. In einem zweiten Kollektiv (n= 26) war im Durchschnitt 5,4 Jahre zuvor die Operation der Stammvarikose vorgenommen worden. Bei der Kontrolluntersuchung liess sich eine Reduktion der Durchmesser von 18,9 mm auf 14,9 mm in der V. poplitea und von 16,5 mm auf 14,7 mm in der V. femoralis superficialis feststellen. Die Dekompensation der tiefen Leitvenen hatte sich also mit der Zeit wieder erholt.
Die Langzeitstudie von Stranzenbach und Hach gibt über das Schicksal der sekundären Leitveneninsuffizienz eine statistisch signifikante Auskunft (31): Nach der klassischen Operation mit korrekter Krossektomie und stadiengerechtem Stripping kommt es zu einer Besserung oder Normalisierung der Strömungsbedingungen in den tiefen Leitvenen.
Krosse-Rezidiv nach Standardoperation
Als Ursache der Rezidivvarikose nach Krossektomie sind 3 morphologische Situationen denkbar, der belassene kurze Stumpf, das inguinale Varizenbeet und die Neovaskularisation (15). Vielleicht erscheint an vierter Stelle noch die „Unberührte Krosse“ nach den neuen Operationsmethoden berechtigt.
Belassener Stumpf
Die konventionelle Operationstechnik fordert eine glatte Ligatur („flush ligation“) der saphenofemoralen Konjunktion. Beim belassenen Stumpf handelt es sich demnach um einen Operationsfehler, der sich durch eine zweite Operation korrigieren lässt (15).
Das inguinale Varizenbeet ist mit der besonderen anatomischen Situation der Leistenregion in Verbindung zu bringen. Bei der routinemäßigen phlebographischen Diagnostik der früheren Jahre war es ein allbekanntes typisches Erscheinungsbild, eine Röntgendiagnose. Die ausgeprägte Erweiterung der V. saphena magna bei einer schweren Varikose überträgt sich natürlich auf alle in die Krosse einmündenden kleinen Venen. Die retrograden Refluxe werden mit Gewalt in die zarten Gefäßnetze hineingepresst und verursachen ihre Umbildung in Krampfadern und die Kommunikation mit anderen großen Venenplexus bis in den Unterbauch und in die Genitalregion hinein (15)
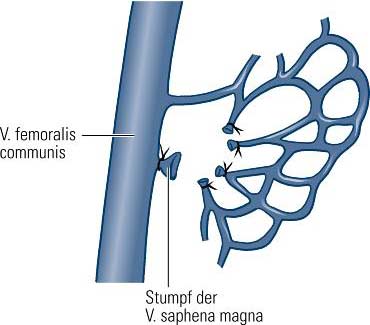 Schematische Vorstellung über die Entstehung des inguinalen Varizenbeets. Nach der Krossektomie bleiben die varikös veränderten Venenäste hinter ihrer Ligatur miteinander in netzförmigen Verbindungen und füllen sich beim Valsalva-Test von irgendwoher auf (aus Hach et al. VenenChirurgie (15))
Schematische Vorstellung über die Entstehung des inguinalen Varizenbeets. Nach der Krossektomie bleiben die varikös veränderten Venenäste hinter ihrer Ligatur miteinander in netzförmigen Verbindungen und füllen sich beim Valsalva-Test von irgendwoher auf (aus Hach et al. VenenChirurgie (15))
Das inguinale Varizenbeet ist also bereits vor der Operation vorhanden. Wegen seiner starken Verzweigungen lässt es sich durch die Ligaturen hinter den Bifurkationen der Krosse-Äste nicht konsequent ausschalten. Auch das „Absuchen“ der V. femoralis communis nach anderen kleinen Abgängen, die das inguinale Varizenbeet speisen, vermag seine Persistenz nicht zu verhindern Garner et al. machten in der Hauptsache die V. saphena accessoria lateralis für das Leistenrezidiv nach Operation verantwortlich (6).
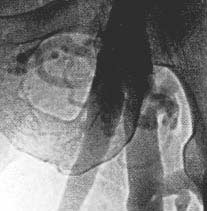
Inguinales Varizenbeet bei einer schweren Stammvarikose der V. saphena magna (links im Bild). Groß- und kleinkalibrige variköse Gefäße in netzförmiger Struktur, die auch nach der Krossektomie erhalten bleiben, dann aber keine wesentliche hämodynamische Bedeutung mehr haben.
Studie. Unter 216 operierten Extremitäten konnten Garner et al. (2003) bei der Kontrolluntersuchung nach 3 Jahren in 141 Fällen (65%) eine Rezidivvarikose in der Leiste durch Duplexsonographie nachweisen. In 61 Fällen (41%) war dafür eine persistierende variköse V. saphena accessoria lateralis verantwortlich zu machen, die schon vor der Operation bestand. This vein „often receives one or more of the lateral abdominal tributaries before joining the saphenofemoral junction. It is often comparable in size to the main saphenous vein“.
Anmerkung. Hier wird in etwa das „inguinale Varizenbeet“ beschrieben und in seiner Bewertung dem Prozess der Neovaskularisation vorangestellt. Die wichtige Arbeit hätte durch phlebographische Dokumentationen und durch hämodynamische Messungen in ihrem Aussagewert profitiert, zumal ja eine deutliche Ausweitung des Eingriffs über die übliche Krossektomie hinaus resultiert.
Bei der Durchsicht von Phlebogrammen zeigt sich immer wieder, dass einzelne Äste des inguinalen Varizenbeets erhebliche Lumina erreichen können und dann mit anderen Venen zu verwechseln sind. Bei der Duplexsonographie bestehen die Refluxphänomene innerhalb dieser Venennetze mitunter schon gleich nach der Krossektomie fort.
Eine in mehrfacher Hinsicht aufschlussreiche Arbeit stammt von Fischer et al. aus St. Gallen (4). Reinhard Fischer ist den deutschsprachigen Venenchirurgen persönlich von seiner jahrzehntelang propagierten „korrekten Krossektomie“ her bekannt ist.
Studie. Fischer et al. nahmen bei 77 von ihm persönlich in der klassischen Weise operierten Patienten (n = 125 Extremitäten) nach 34 Jahren eine Nachuntersuchung mit der Duplexsonographie vor. Davon wiesen 53 Extremitäten (42,4%) ein echtes Krosserezidiv auf, entweder mit diffusem, meist kleinkalibrigem Varizenstrang (n= 22, Typ B1; 17,6% ) oder mit einläufiger Varize (n = 31, Typ B2; 24,8%). Außerdem fanden sich „benachbarte Insuffizienzen“ bei 22 (17,6%) Extremitäten (Pseudorezidiv; Typ C).
Anmerkung. Die 3 verschiedenen Formen der Rezidivvarikose nach Fischer ließen sich unter den Begriffen des inguinalen Varizenbeets und der Neoangiogenese einordnen. Kurze belassene Stümpfe der V. saphena magna, also „Operationsfehler“, wurden nicht mitgeteilt. Jedoch erfolgte die Durchtrennung der mündungsnahen Seitenäste ohne Mitnahme der ersten Verzweigung, und die V. pudendalis externa profunda wurde nur ausnahmsweise ligiert. Es blieben also relativ große Gefäße in dem inguinalen Varizenbeet zurück. Dafür erfolgte die Inspektion der V. femoralis auf eine Instanz von 1 cm.
Schlussfolgerung. Fischer bezeichnete 25 der 31 Rezidive aus dem Kollektiv B2 (Neoangiogenese) als klinische relevant, ohne dass jedoch der Beweis für die Relevanz durch physikalische Messungen erbracht wurde. Möglicherweise hatte die sparsame Krossektomie aber ein größeres inguinales Varizenbeet zur Folge (Kollektiv C).
Zu ähnlichen Ergebnissen kam schon das Consensus-Meetung der französisch- und englisch-sprachigen Phlebologen am 17.-18. Juli 1998 in Paris unter der Leitung von Perrin (26). Die Häufigkeit der Rezidivvarikose im Leistenbereich lag bei 20 bis 80% innerhalb 5 bis 20 Jahre nach der Operation. Sie nahm mit der Zeitspanne nach dem Eingriff zu. Die operative Technik (vor der endovasalen Chirurgie) umfasste die „französische Krossektomie“ mit flush-ligation der saphenofemoralen Junktion sowie der Durchtrennung aller einmündenden Äste hinter ihrer ersten Bifurkation, und dann das Stripping-Manöver. In der Pathogenese der Rezidivvarikose wurden Fehler der Erstbehandlung, aber nicht das inguinale Varizenbeet angesprochen.
Die Neoangiogenese steht heute im Brennpunkt der Diskussionen (5). Die ersten Beobachtungen gehen schon auf von Langenbeck 1860 (18) und vor allem auf Ledderhose 1904 (19) zurück. Der Belfaster Chirurg Glass hat das Thema 1987 durch klinische und experimentelle Untersuchungen wieder aktualisiert (10 - 12). Im deutschen Sprachraum befasst sich besonders die Arbeitsgruppe um Frings damit (7, 8). Die kleinen Gefäße der Neoangiogenese gehen von der Intima des abgetrennten Saphenatrichters oder von lymphovenösen Anastomosen aus. Eine andere Theorie beruht auf der Aktivierung von Wachstumsfaktoren (Literatur bei Haas et al 2005 (13)). Die Gefäße sind morphologisch durch ihre ungewöhnlich starke Schlängelung charakterisiert (3, 25). Schon allein von dieser Feststellung her ist eine relevante Strömung von größeren Blutvolumina auszuschließen. Demnach können Neovaskulate einen pathologischen Rezirkulationskreis nicht aufrecht erhalten oder sogar induzieren. Das bedeutet mit anderen Worten, dass sie in Hinsicht auf eine sekundäre Leitveneninsuffizienz keine klinische Relevanz haben. Allerdings beurteilt Frau De Maeseneer diese Situation kontrovers (3).
 Neovaskularisation in der Leiste nach korrekter Krossektomie ohne Stripping der V. saphena magna. Stark geschlängeltes Neovaskulat von der V. femoralis communis bis zum Saphena-Stumpf. Zeichnung aus der Arbeit von De Maeseneer (3).
Neovaskularisation in der Leiste nach korrekter Krossektomie ohne Stripping der V. saphena magna. Stark geschlängeltes Neovaskulat von der V. femoralis communis bis zum Saphena-Stumpf. Zeichnung aus der Arbeit von De Maeseneer (3).
Wegen ihres geschlängelten Verlaufs und der dadurch bedingten starken Abbremsung der Blutströmungsgeschwindigkeit bilden sich die Gefäße einer Neoangiogenese bei der aszendierenden Pressphlebographie in der Leiste oftmals schlecht, in der Kniekehle aber besser ab. Sie sind vor allem eine Erkenntnis der duplexsonographischen Refluxdiagnostik (15). In histologischer Hinsicht lassen sie sich durch multiple Lumina, durch den unregelmäßigen Aufbau der Venenwände und durch das Fehlen von Venenklappen gegenüber genuinen Krampfadern unterscheiden (24).
 Neovaskularisation mit sehr stark geschlängelten Gefäßkonvoluten in der Kniekehle nach 4-maliger Operation bei einer 53-jährigen Patientin. Kasuistik von Frau Dr. Haas, Schlossklinik am Abtsee. Wir bedanken uns für die Überlassung der Phlebogramme.
Neovaskularisation mit sehr stark geschlängelten Gefäßkonvoluten in der Kniekehle nach 4-maliger Operation bei einer 53-jährigen Patientin. Kasuistik von Frau Dr. Haas, Schlossklinik am Abtsee. Wir bedanken uns für die Überlassung der Phlebogramme.
Unberührte variköse Krosse in den Stadien III und IV
Keine der drei genannten Konstellationen ist mit einer „unberührten varikösen Krosse“ zu vergleichen, wie sie bei den endovasalen (und besonders den gefäßerhaltenden) Operationsmethoden im Falle der Stammvarikose in den Stadien III und IV hinterlassen wird. In dieser Situation kann unter der Valsalva´schen Exposition ein hohes Strömungsvolumen in das weit verzweigte Venennetz des Beins refluktieren. Der Prozess wird klinisch relevant, sobald sich in der Peripherie der Anschluss an ein „Aufnahmegefäß“ ergibt. Hierfür kommen die Doppelungen der Saphena-Venenstämme am Bein in Betracht, die sich außerordentlich häufig finden (15). Aber systematische Untersuchungen dieser Zusammenhänge stehen aus.
Verlauf der Stammvarikose nach Operation
Entscheidend für den Verlauf der Krampfaderkrankheit nach der Operation ist die präoperative phlebologische Situation, genauer gesagt, das Ausmaß der sekundären Leitveneninsuffizienz. Im Stadium I, also der Seitenastvarikose der V. saphena accessoria lateralis, und im Stadium II wirkt sich die Varikose nicht im Sinne einer sekundären Leitveneninsuffizienz aus, auch nicht bei jahrzehntelangem Verlauf. Deshalb bleibt es bezüglich des Rezirkulationskreises ganz gleich, ob die Varikose behandelt wird oder nicht, und auch, wie sie behandelt wird. Es muss in Anbetracht der persistierenden insuffizienten transfaszialen Kommunikationen lediglich mit einer höheren Rezidivquote von Krampfadern gerechnet werden, nicht aber mit der Dekompensation von Rezirkulationskreisen. Dagegen können die Rezirkulationskreise III und IV ohne Operation im klassisschen Sinne früher oder später zur sekundären Leitveneninsuffizienz führen und dann ein langzeitiges und komplikationsträchtiges Krankheitsbild nach sich ziehen.
Ein begrenztes refluktierendes Blutvolumen bei selektiv belassener Krosse ist zwar nicht in der Lage, eine sekundäre Leitveneninsuffizienz neu entstehen zu lassen. Es vermag aber, einen bereits eingefahrenen dekompensierten Rezirkulationskreis aufrecht zu erhalten, bzw. seine Rückbildung zu verhindern.
Der Schweizer Dermatologe Hofer formulierte die Frage des Magna-Rezidivs aus heutiger Sicht in einer interessanten Version: „Ist es möglich, dass durch alleinige endovenöse Obliteration der epifaszialen Stammvarize ohne offene Krossektomie die Häufigkeit des Magna-Rezidivs vermindert werden kann, weil keine Reize zur Stimulation der Neovaskularisation gesetzt werden“? (16).
Studie. Von 1996 bis 2003 wurden von Hofer 1165 Stammvarikosen nach der klassischen Methode operiert, deren Diagnose durch die Duplexsonographie und die Plethysmographie gesichert waren. In 50% der Fälle lagen pathologische Werte der Plethysmographie mit T0 <19 vor. Darunter befanden sich auch 100 Extremitäten mit einer Rezidivvarikose, die von einem isolierten Magna-Krosserezidiv ausgingen (Kollektive MKR). Wenn ein in situ gelegener Magnastamm oder ein kalibermäßig vergleichbares Gefäß vorlagen, betrug die Frequenz der pathologischen Messwerte 50% (n = 46), ohne Magnastamm 27,6% (n = 29) und mit isolierter Varize der V. saphena accessoria lateralis 20% (n = 25). Die Zweitoperation wurde nur bei pathologischen Messwerten für angezeigt gehalten.
Anmerkung. Hofers Ergebnisse lassen sich durch die theoretische Konzeption des inguinalen Varizenbeetes und des Rezirkulationskreises einfach erklären. Die relativ hohe Anzahl von pathologischen Messwerten im Gesamtkollektiv von 43,2% weist darauf hin, dass auch viele Patienten mit sekundärer Leitveneninsuffizienz in die Statistik eingeschlossen sind.
Schlussfolgerung. Die Krossektomie hat in der Chirurgie der Stammvarikose einen wichtigen Platz.
Auch Recek hat seine Nachuntersuchungen mit der Funktionsdiagnostik korreliert und damit beweisen können, dass bei der klinisch relevanten Stammvarikose die Krossektomie eine wichtige hämodynamische Bedeutung hat (30).
Studie. Im Jahre 2000 veröffentliche Recek die Spätergebnisse nach Krossektomie (n = 70 Extremitäten) und ineffektiver postoperativer Sklerosierung (davon 81,5%), d.h. bei erhaltenem varikösen Venenstamm. Die Ergebnisse wurden bis zu 4 Jahre anhand der Strain-gauge-Plethysmographie und der Duplexsonographie kontrolliert. Nach der Operation kam es zunächst zu einer Verbesserung der Auffüllzeiten und dann wieder langsam zur Verschlechterung, während sich die Auffüllvolumina, die das wichtige Maß für die Pumpfunktion darstellen, mit hoher statistischer Signifikanz konstant hielten.
Schlussfolgerung. Die Krossektomie allein hat einen über 4 Jahre nachgewiesenen statistisch hoch signifikant günstigen Einfluss auf die Hämodynamik bei persistierender Stammvarikose.
Problemstellung der endovasalen Operationen
Letztendlich dürfte es sich auf den Behandlungserfolg einer Stammvarikose nicht auswirken, auf welche Weise der varikös degenerierte Abschnitt der Stammvene aus dem Rezirkulationskreis ausgeschaltet wird, durch mechanische Entfernung (Stripping), durch Koagulation (Laser, Radiofrequenz-Ablation) oder durch Sklerosierung. In jedem Fall lässt sich die erfolgreiche Eliminierung des varikösen Venenstamms auf einfache Weise durch die farbkodierte Duplexsonographie dokumentieren.
Unter Berücksichtigung der pathophysiologischen Bedingungen und der nunmehr Jahrhunderte alten Erfahrungen mit der „korrekten“ Krossektomie erscheint es notwendig, die in der Literatur durchweg als gut evaluierten Ergebnisse der neuen endovasalen Operationsmethoden ohne Krossektomie kritisch zu beleuchten. Natürlich muss der Langzeiteffekt dabei noch außer Acht gelassen werden.
Radiofrequenz-Ablation (VNUS-Technik)
Die Arbeit von Merchant et al. ist zwar schon etwas älter, aber genau nachzuvollziehen (21).
Studie. In die multizentrische Studie von Marchant et al. (2002) wurden 319 Extremitäten zur „Ausschaltung des Saphena-Refluxes“ durch Katheterobliteration (VNUS-Technik) einbezogen. Nach 24 Monaten konnte ein kompletter Verschluss der Krosse in 85,2%, ein nahezu kompletter Verschluss (offenes Lumen < 5 cm Länge) in 3,5% und eine Rekanalisation (offenes Lumen > 5 cm Länge) in 11,3% nachgewiesen werden. Die CEAP-Klassifikation erlaubte die Analyse des Krankengutes: In 5% handelte es sich um die Merkmale C0-1, in 69,9% um C2, in 8,2% um C3 und nur in 17% um die Kriterien C4-6.
Anmerkung. Messergebnisse der venösen Hämodynamik wurden in die Studie nicht eingebracht, ebenso wenig die Einteilung in Stadien. Rückschlüsse auf das Verhalten der Rezirkulationskreisläufe und damit auf die Schwere der Erkrankung in den einzelnen Kollektiven sind deshalb nicht möglich. Weniger als jeder 5. Fall gehörte nach der CEAP-Nomenklatur zu den „komplizierten Varikosen“.
Bei vergleichenden Betrachtungen des Quality-of-life-Scores (EVOLVeS-Studie) zwischen der Radiofrequenz-Ablation ohne Krossektomie und der konventionellen Stripping-Operation mit Krossektomie ergab sich erwartungsgemäß ein Vorteil zugunsten der ersteren Gruppe (20).
Studie. In der EVOLVeS Studie (2003) wurden die Operation und der perioperative Zeitraum nach dem Erlebnisgefühl der Patienten analysiert, und zwar bei 44 Extremitäten nach der Closure- und bei 36 nach der Standard-Methode. Es handelte sich um Stammvarikosen der V. saphena magna C2-4 , und zwar 81,8% bzw. 77,8% in C2, 9,1% bzw. 11,1% in C3 und ebensoviel in C4.
Anmerkung. Die gleichmäßig in beiden Kollektiven ausgeschalteten Venensegmente von 37 + 2 cm bzw 40 + 2 cm sprechen möglicherweise dafür, dass die Einteilung nach Stadien keine Anwendung erfuhr, und dass die Verhältnisse der Rezirkulationskreisläufe nicht beachtet wurden. Nur jeder 9. Fall hatte eine „komplizierte Varikose“.
Laser-Koagulation
Seit Einführung der endoluminären Laser-Koagulation 1999 (1) liegen bereits mittelzeitige Behandlungsergebnisse mit dieser Methode vor. Dabei geht es in der Diskussion besonders um die Frage, ob eine Krossektomie zur Prophylaxe des Krosserezidivs notwendig ist oder nicht (22). In einem Konsensus am 10. Januar 2004 wurde die indikatorische Zielrichtung als die gleiche gesehen wie für die klassische Operation mit Krossektomie und Stripping (28, 29).
Studie. Im Jahre 2003 berichtete Proebstle über die Kontrolluntersuchung von 508 Laser-Eingriffen nach 12 Monaten, davon 345 an der V. saphena magna. Die Krankheit entsprach den Merkmalen C2-C4, aber auch C5 (4%) und C6 (13%). Rekanalisierungen wurden in 5 Fällen und Teilrekanilisationen in weiteren 5 Fällen registriert, wahrscheinlich infolge einer Unterdosierung der Laser-Energie.
Anmerkung. Es erfolgten keine näheren Angaben über die Charakteristika des Krankenguts, insbesondere über den Schweregrad der Stadien und über das Vorliegen einer sekundären Leitveneninsuffizienz. Das der Arbeit beigefügte Sonogramm der Krosse vom ersten postoperativen Tag zeigt erhaltene Seitenäste.
Studie. Im Jahre 2003 veröffentlichten Min et al. ihre Erfahrungen an 499 Patienten im Verlaufe von 3 Jahren. Beim Follow-up nach 2-Jahren lag die Rezidivquote bei 7% (Extremitäten n = 504). Einzelheiten über das Patientengut hinsichtlich spezieller Indikationen sind im Detail nicht aufgeführt.
Schlussfolgerung
Die Beurteilung verschiedener Operationsmethoden hinsichtlich ihrer Effektivität zur Vermeidung der chronischen venösen Insuffizienz beruht letztendlich auf der Ausschaltung bzw. der Prophylaxe der sekundären Leitveneninsuffizienz. Bei dieser Betrachtung wird nach unserer Meinung dem Rezidiv in der Leistenregion eine zentrale Bedeutung zuerkannt. Heute ist die klassische Chirurgie der Stammvarikose hinsichtlich ihrer präoperativen Diagnostik und Technik so weit fortgeschritten und als Erfahrungsgut anerkannt, dass mit operativen Fehlern im Sinne belassener Stümpfe, wie sie bis vor wenigen Jahren eine erhebliche Rolle gespielt haben, kaum mehr zu rechnen ist. Ganz im Vordergrund der Rezidivvarikose steht deshalb das Konzept des inguinalen Varizenbeetes, das im Verständnis der Pathophysiologie noch nicht überall seine gebührende Bedeutung erfahren hat. Gerade die intravasalen Operationsmethoden laufen Gefahr, sich an diesen Maßstäben vorbei zu entwickeln.
Als Grundlage der Chirurgie einer Stammvarikose gelten die bisher nicht widersprochenen Konzeptionen der Rezirkulationskreise und ihrer Dekompensation zur sekundären Leitveneninsuffizienz. Hierfür müssen die Stadien III und IV der V. saphena magna sowie die Stadien II und III der V. saphena parva verantwortlich gemacht werden. Nur in der Kombination mit der Krossektomie kann die Ausschaltung des Venenstamms einen pathologischen Rezirkulationkreislauf dauerhaft unterbrechen. Alle anderen Formen von Rezidivvarizen, die sich im späteren Leben unweigerlich einstellen, haben keine größere hämodynamische Bedeutung. Aus dem theoretischen Verständnis und der praktischen Erfahrung heraus sind weder das inguinale Varizenbeet noch die Gefäße der Neoangiogenese einer chirurgischen Behandlung wirklich zugänglich. Sie bedürfen keiner zweiten Krossektomie und kommen gegebenenfalls mit der Sklerosierung oder mit der Miniphlebektomie aus.
Oft gelangen Patienten mit einer Stammvarikose der Stadien I und II zur Behandlung. Hier konnte bisher nicht nachgewiesen werden, dass die Krankheit zu Veränderungen der Hämodynamik im Sinne der sekundären Leitveneninsuffizienz führt, auch nicht nach langjähriger Persistenz im höheren Lebensalter. In der Therapie stehen ästhetische Aspekte absolut im Vordergrund. Gegen die Anwendung der klassischen, der endovasalen und extravasalen Operationsmethoden oder gegen die Schaumsklerosierung ist sachlich nichts einzuwenden. Der Patient sollte aber darüber informiert werden, dass ihm auch ohne jegliche chirurgische Therapie keinerlei Nachteile von den Krampfadern entstehen.
Eine vergleichende prospektive Studie zur Bewertung der neuen Operationsmethoden mit und ohne Krossektomie erscheint dringend geboten. Dabei sind vor allem auch die Parameter der sekundären Leitveneninsuffizienz in Abhängigkeit von den unterschiedlichen Kriterien der Stammvarikose zu verfolgen.
Literaturverzeichnis
1. Boné C. Tratamiento endoluminal de las varices con laser de diodo: estudio preliminary. Rev Patol Vasc 1999; 5: 35-46
2. Breu FX, Guggenbichler S, Marshall M. Konsensuskonferenz zur Schaumsklerosierung. Phlebol 2004; 33: 97-105
3. De Maeseneer MGR. The role of postoperative neovascularisation in recurrence of varicose veins: from historical background to today´s evidence. Acta Chir Belg 2004; 104: 283-9
4. Fischer R, Linde N, Duff C, Jeanneret Ch, Seeber P. Das Krosserezidiv – eine Nachkontrolle nach 34 Jahren. Phlebol 2000; 29:17-22
5. Fischer R, Kluess G, Frings N, Duff C. Der aktuelle Stand der Magnakrossenrezidiv-Forschung. Phlebol 2003; 32: 54-9
6. Franceschi C. Théorie et pratique der la cure conservatrice et hémodynamique de l´insuffisance veineuse en ambulatoire. Armoncon, Précy-sous-Thil, 1988
7. Frings N, Tran VTP, Nelle A, Glowacki P. Krossenrezidiv der V. saphena magna trotz korrekter Krossektomie: Neoangiogenese. Phlebol 1999; 28: 144-8
8. Frings N, Nelle A, Tran VTP, Glowacki P. Unvermeidbnares Rezidiv und Neoreflux nach korrekter Vena-saphena-magna-Krossektomie: Neovaskularisation? Phlebol 2003; 32: 96-100
9. Garner JP, Heppel PSJ, Leopold PW. The lateral accessory saphenous vein – a common cause of recurrent varicose veins. Ann R Coll Surg Eng 2003; 85: 389-92
10. Glass GM. Neovascularisation in recurrence of the varicose great saphenous vein following transsection. Phlebology 1987; 2: 81-91
11. Glass GM. Neovascularisation in restauration of continuity of the rat femoral vein following surgical interruption. Phlebology 1987; 2: 1-6
12. Glass GM. Neovascularisation in recurrence of varices of the great saphenous vein in the groin: phlebography. Angiology 1988; 39: 577-82
13. Haas E, Burkhardt T, Maile N. Rezidivhäufigkeit durch Neoangiogenese nach modifizierter Krossektomie. Phlebol 2005; 34: 101-4
14. Hach W. Untersuchungen des extrafaszialen Venensystems unter besonderer Berücksichtigung der aszendierenden Pressphlebographie. Demeter. Gräfelfing 1981
15. Hach W, Gruss J, Hach-Wunderle V, Jünger M. VenenChirurgie. Schattauer. Stuttgart New York 2005
16. Hofer T. Rezidivvarizen: Progression der Varikosis. Phlebol 2004; 33: 186-90
17. Jessup G, Lane RJ. Repair of incompetent venous valves: a new technique. J Vasc Surg 1988; 8:569-75
18. Langenbeck B von. Beiträge zur chirurgischen Pathologie der Venen. Arch Klin Chir 1861; 1: 80
19. Ledderhose G. Über die Regeneration der unterbundenen Saphena. Dt Zeitschr Chir 1904; 71: 401-8
20. Lurie F, Creton D, Eklof B, Kabnick LS, Kistner RL et al. Prospective randomized study of endovenous radiofrequency obliteration (Closure procedure) versus ligation and stripping in a selected patient population (EVOLVEeS Study). J Vasc Surg 2003; 38: 207-14
21. Merchant RF, DePalma RG, Kabnick LS. Endovascular obliteration of saphenous reflux: A multicenter study. J Vasc Surg 2002; 35: 1190-6
22. Min RJ, Khilnani N, Zimmet SE. Endovenous Laser treatment of saphenous vein reflux: Long-term results. J Vasc Interv Radiol 2003; 14: 991-6
23. Moro G. Ueber die Pathogenese und die zweckmäßigste Behandlung der Krampfadern der unteren Extremitäten. Beitr Klin Chir 71;1910: 420-35
24. Mumme A, Olbrich S, Barbera L, Stücker M. Saphenofemorales Leistenrezidiv nach Stripping der Vena saphena magna: technischer Fehler oder Neovaskularisation. Phlebol 2002; 31: 38-41
25. Mumme A, Olbrich S, Barbera L, Geier B, Stücker M. Validität der makroskopischen Identifikation von Neovaskulaten durch den Operateur. Phlebol 2003; 32: 143-6
26. Perrin MR, Guex JJ, Ruckley CV, dePalma RG, Royle JP et al. Recurrent varices after surgery (REVAS), a consensus document. Cardiovasc Surg 2000; 8:233-45
27. Perthes G. Ueber die Operation der Unterschenkelvaricen nach Trendelenburg. Dtsch Med Wochenschr 21; 1895: 253-7
28. Proebstle TM, Pannier FM, Schuller-Petrovic S, Offermann M, Hohenleutner U, Rabe E. Konsensus zur endovenösen Lasertherapie der Varikose. Phlebol 2004; 33: 106-9
29. Proebstle TM. Endovenöse Lasertherapie der Varikose. Phlebol 2003; 32: 131-7
30. Recek C. Spätergebnisse nach Krossektomie und Sklerotherapie. Phlebol 2000; 29: 23-6
31. Stranzenbach W, Hach W. Phlebographische Verlaufsbeobachtungen der sekundären Popliteal- und Femoralveneninsuffizienz bei Stammvarikose. Phlebol 1991; 20: 25-9
32. Trendelenburg T. Ueber die Unterbindung der Vena saphena magna bei Unterschenkelvaricen. Beitr Klin Chir 7, 1891: 195-210
zum Anfang
zurück

